全流程管控,全速助力 医药新产品卓越上市的教育管理新策略
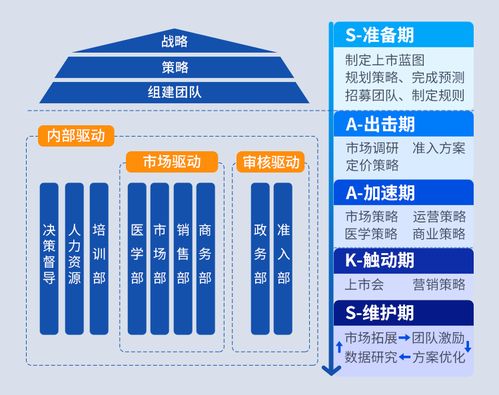
在当今竞争激烈的医药市场中,新产品的成功上市不仅关乎企业的商业回报,更直接影响到公众健康福祉的实现。从实验室的曙光初现,到最终惠及广大患者,这段旅程充满了科学、法规与市场的多重挑战。因此,构建一套系统化、精细化且高效敏捷的“全流程管控”体系,并深度融合前瞻性的“教育管理”策略,已成为驱动医药新产品卓越上市、实现全速推进的核心引擎。
一、 全流程管控:铸就上市成功的坚实骨架
医药新产品的上市绝非一蹴而就,它是一个环环相扣、涉及多部门协作的漫长链条。全流程管控意味着对从早期研发、临床前研究、临床试验、注册申报、生产准备、市场准入到上市后监测的每一个关键节点进行前瞻性规划、动态监控与闭环管理。
- 早期规划与战略协同: 在产品研发早期,即需引入市场、准入、医学、合规等多部门视角,共同制定清晰的上市目标与路径图。这确保了科学探索与商业及患者需求同频共振。
- 临床开发与证据生成: 以终为始,设计能够满足核心市场(如中国NMPA、美国FDA、欧盟EMA)注册要求,并能有力支撑产品差异化价值的临床试验方案。高效的临床运营管理与数据质量管控是确保项目按时、高质量推进的基石。
- 注册申报与法规导航: 组建精通全球法规的专业团队,与监管机构保持积极、透明的沟通。通过科学的注册策略,加速审评进程,应对复杂的法规环境变化。
- 供应链与生产准备: 确保在获批前,商业化生产体系(包括原料、工艺、质量、产能)已准备就绪,满足GMP要求,保障产品稳定、可靠的供应。
- 市场准入与价值传递: 深度理解支付方(医保、商保)、医疗机构及患者的需求,提前布局卫生经济学研究、价格谈判与医保目录准入策略,确保产品可及性与可负担性。
二、 教育管理:注入全速上市的核心动能
如果说全流程管控构建了上市的“硬件”骨架,那么贯穿始终的“教育管理”则是激活全局、提升效率、规避风险的“软件”灵魂。这里的“教育”是广义的,包含对内赋能与对外沟通两个维度。
- 对内赋能:打造高绩效上市团队
- 跨职能知识融合: 定期组织研发、医学、市场、销售、准入、合规等部门的联合培训与研讨会,打破部门墙,确保所有团队成员对产品科学、战略定位、目标患者、竞争格局及法规要求有统一、深刻的理解。
- 情景模拟与技能演练: 针对关键节点(如专家咨询会、医保谈判、危机公关),进行模拟演练,提升团队应对复杂局面的实战能力与协同效率。
- 文化塑造与目标对齐: 通过持续的内部沟通,将“以患者为中心”、“合规先行”等核心理念深植团队,确保所有行动与上市战略目标高度一致。
- 对外沟通:构建信任与理解的桥梁
- 关键意见领袖(KOL)与医疗专业人士教育: 通过学术会议、研讨会、医学交流项目等,基于坚实的临床证据,科学、客观地传递产品的创新价值、作用机制及临床应用前景,建立专业领域的认知与认可。
- 患者教育与疾病管理: 开发易于理解的患教材料,帮助患者及其家属正确认识疾病与治疗方案,提升治疗依从性,同时收集真实世界反馈,优化产品与服务。
- 支付方与政策制定者沟通: 通过翔实的数据和符合国情国策的价值论证,向支付方清晰阐述产品带来的临床获益、经济价值与社会效益,为顺利准入铺平道路。
- 公众科普与媒体关系管理: 适时、适度地进行公众科普,提升疾病认知,塑造负责任的创新企业形象,为产品上市营造良好的社会舆论环境。
三、 融合与协同:实现“全速助力上市”的飞轮效应
“全流程管控”与“教育管理”并非两条平行线,而是深度融合、相互促进的有机整体。例如,在临床开发阶段(管控环节),对研究者团队的高效培训(教育环节)能显著提升试验质量和入组速度;在市场准入阶段(管控环节),对支付方决策者的精准价值沟通(教育环节)是成功准入的关键。
通过将系统性的教育管理深度嵌入每一个管控节点,企业能够:
- 提升决策质量与执行效率: 知识共享减少内耗,加速共识形成。
- 有效管控风险: 提升全员合规意识,前瞻性识别并应对潜在危机。
- 最大化产品价值: 确保从研发到商业化的每一个环节,都在为产品的最终市场成功和患者获益增值。
- 构建长期竞争优势: 培养一支专业、协同、有战斗力的团队,并积累宝贵的组织知识与信任资本。
结论
医药新产品的卓越上市,是一场需要科学匠心、商业智慧与人文关怀并举的复杂交响。唯有构建坚如磐石的“全流程管控”体系,并灌注以充满活力的“教育管理”动能,实现“硬骨架”与“软灵魂”的完美融合,才能真正做到“全速助力上市”,让每一份创新都能安全、高效、精准地抵达需要的患者手中,兑现医药行业造福人类健康的庄严承诺。
如若转载,请注明出处:http://www.jieyuekt.com/product/13.html
更新时间:2026-06-05 10:41:39